Tabla de enlaces
Resumen e I. Introducción
-
Materiales y métodos
2.1. Aprendizaje de instancias múltiples
2.2. Arquitecturas de modelos
-
Resultados
3.1. Métodos de entrenamiento
3.2. Conjuntos de datos
3.3. Tubería de preprocesamiento de WSI
3.4. Resultados de clasificación y detección de ROI
-
Discusión
4.1. Tarea de detección de tumores
4.2. Tarea de detección de mutaciones genéticas
-
Conclusiones
-
Expresiones de gratitud
-
Declaración y referencias del autor
4. Discusión
4.1. Tarea de detección de tumores
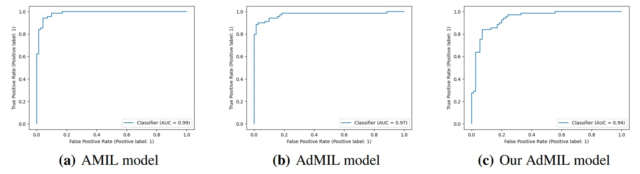
Los modelos se desempeñaron a la par con el estado del arte para esta tarea, en términos de su capacidad para clasificar correctamente WSI, con valores AUC superiores a 0.9 (Tabla 1). El artículo unique [7] Usó dos conjuntos de datos de imágenes H&E: el conjunto de datos de cáncer de mama y el conjunto de datos de cáncer de colon. Comparando nuestros resultados con los reportados en este trabajo, obtuvimos resultados significativamente mejores que los primeros resultados y similares a los segundo. Sin embargo, debemos tener en cuenta que estos conjuntos de datos no solo son
de un tipo de cáncer diferente pero también compuesto de parches como bolsas, en lugar de diapositivas. Otros trabajos utilizaron la arquitectura AMIL y sus propias variaciones con conjuntos de datos compuestos de mosaicos a mayores magnificaciones [11, 20]. En normal, obtuvimos un AUC mejor que el trabajo previo informado, lo que respalda el hecho de que el aumento de 5X podría ser adecuado para identificar tumores.
Teniendo en cuenta que el conjunto de datos que utilizamos solo tenía diapositivas con flash congelados, que presentaba algunos artefactos, y que incluía porcentajes variados de tumores, podemos suponer que los modelos aprendieron a diferenciar factores no relacionados de los tumores presentes en las imágenes. Además, estos resultados se obtuvieron de los mosaicos con un aumento de 5x, un nivel que muestra tejido pero no células. Esto respalda la hipótesis de que, al igual que los patólogos, los modelos pueden aprender a identificar los portaobjetos tumorales a nivel de tejido. También revela que la tarea en sí misma podría no ser lo suficientemente desafiante, y explorar mayores magnificaciones no mejorará significativamente la capacidad de clasificación de las diapositivas. Se debió a estos resultados y al hecho de que este es el nivel más común utilizado para la detección de tumores por parte de los patólogos de que no exploramos más niveles de aumento para esta tarea.
Al analizar los puntajes de atención producidos, observamos que tanto la arquitectura AMIL (Figura 7 (b)) como nuestra versión del modelo de admilado (Figura 7 (f)) producen puntajes de atención más escasos en comparación con el ADMIL unique (Figura 7 (d)) como predijimos anteriormente. Este comportamiento puede ser especialmente importante si las regiones tumorales (o los ROI deseados) parecen más dispersos. Por otro lado, para las morfologías que generalmente se centran más en un parche específico, la capa de atención del admilado unique podría ser preferible.
Por otro lado, al analizar las puntuaciones excitatorias/inhibitorias producidas por el marco aditivo MIL, las puntuaciones producidas por el modelo de admilado unique tienden a ser positivas para la mayoría de los parches (Figura 7 (c)), mientras que las que producen nuestra versión de Admil solo resaltan una pequeña porción (Figura 7 (E)). Este comportamiento se observó para la mayoría de las diapositivas. Dado que la única diferencia en la arquitectura de los modelos son sus capas de atención, concluimos que los puntajes de atención más escasos tienden a hacer que el clasificador de instancias considere solo un pequeño subconjunto de parches como excitadores. Dependiendo de los resultados adquiridos de una evaluación futura de la relevancia de los mapas de calor, esto podría respaldar la hipótesis de que los puntajes de atención no necesariamente resaltan los ROI deseados y podrían no ser suficientes para la pintura WSI significativa.
También es interesante notar que los puntajes de atención de AMIL tienden a centrarse más en los bordes del tejido (Figura 7 (b)). Esto podría significar que el tumor está presente en los bordes del tejido, pero también podría revelar cierto sesgo en el modelo de parches que incluyen algún porcentaje de antecedentes. Debido a la ampliación utilizada, y las fracturas que aparecen en los portaobjetos con flash congelados, hubo una cantidad significativa de parches que contenían antecedentes, en comparación con las magnificaciones más altas y es posible que esto condicionara la capacidad de aprendizaje del modelo.
Se debe realizar una evaluación adicional de la detección de ROI, especialmente una evaluación cualitativa de los mapas de calor obtenidos. Necesitaríamos la ayuda de los patólogos para confirmar que los puntajes de parche que obtienen estos modelos son indicadores de regiones tumorales. Además, si bien el modelo AMIL mostró un AUC ligeramente mejor que los otros modelos, esto no significa necesariamente que sus mapas de calor sean más relevantes o útiles para los patólogos. Las puntuaciones de parche obtenidas de los otros dos modelos, debido a su naturaleza inhibitoria/excitadora, podrían proporcionar una mayor visión de la presencia tumoral en los portaobjetos. Debido a las limitaciones de tiempo y la inexistencia de los mapas de calor de la verdad terrestre, esta evaluación se deja como un trabajo futuro.
Autores:
(1) Martim Afonso, Instituto Superior Técnico, Universidade de Lisboa, Av. Rovisco Pais, Lisboa, 1049-001, Portugal;
(2) Praphulla MS Bhawsar, División de Epidemiología y Genética del Cáncer, Instituto Nacional del Cáncer, Institutos Nacionales de Salud, Bethesda, 20850, Maryland, EE. UU.;
(3) Monjoy Saha, División de Epidemiología y Genética del Cáncer, Instituto Nacional del Cáncer, Institutos Nacionales de Salud, Bethesda, 20850, Maryland, EE. UU.;
(4) Jonas S. Almeida, División de Epidemiología y Genética del Cáncer, Instituto Nacional del Cáncer, Institutos Nacionales de Salud, Bethesda, 20850, Maryland, EE. UU.;
(5) Arlindo L. Oliveira, Instituto Superior Técnico, Universidade de Lisboa, Av. Rovisco Pais, Lisboa, 1049-001, Portugal e Inesc-ID, R. Alves Redol 9, Lisboa, 1000-029, Portugal.
Este documento es